糖尿病足、外周动脉疾病等引起的组织缺血,是临床致残、致死的重要原因。当肢体供血严重不足,患者不仅面临溃疡、坏疽的痛苦,更时刻面临截肢的威胁。据统计,严重肢体缺血患者术后1年死亡率高达37%,2年死亡率达49%。尽管血管搭桥、介入治疗等手段不断发展,但微循环功能障碍难以修复、慢性创面无法愈合,仍是临床难以攻克的痛点。促血管生成策略虽被视为突破口,但传统生长因子(如VEGF)递送存在半衰期短、易失活、无法持续作用等局限,难以支撑功能性血管网络的稳定构建。

鹿茸作为哺乳动物中唯一能周期性完全再生的器官,其日均生长速度可达2.75厘米,背后是极其旺盛的血管新生能力。受此启发,南京中医药大学王裔惟教授、段金廒教授、刘培副教授团队在化工领域国际期刊《Chemical Engineering Journal》上发表题为“Targeted and sustained release of pilose antler peptide from a thermosensitive injectable hydrogel for ischemic tissue repair”的研究论文。该团队将鹿茸中具有促血管生成活性的多肽(PAP)与温敏水凝胶PNPHO通过共价键结合,构建了一种可注射的长效缓释系统PAP-co-PNPHO。该策略通过精准、持续、可控的递送方式,突破了传统给药局限,为缺血性疾病的治疗提供了新思路。论文第一作者为南京中医药大学赵文健博士、薛楠楠博士后;南京中医药大学刘培副教授、段金廒教授、王裔惟教授为该论文的共同通讯作者。
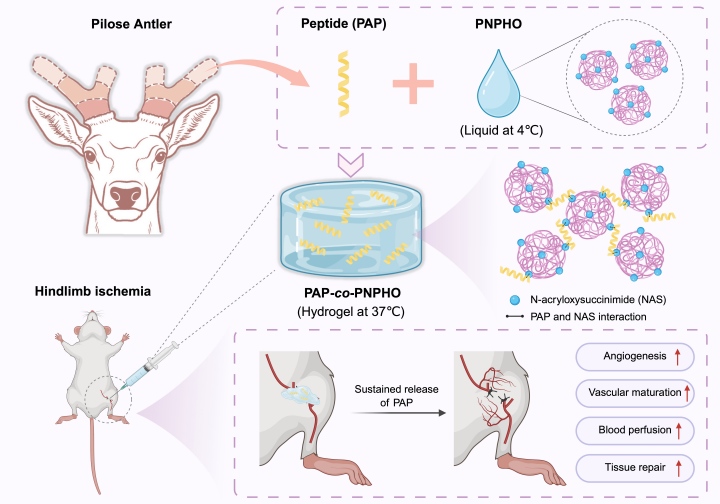 图一、PAP-co-PNPHO温敏水凝胶的构建及其促血管再生示意图
图一、PAP-co-PNPHO温敏水凝胶的构建及其促血管再生示意图
本文要点:
(1)体外实验证实,鹿茸多肽(PAP)能显著促进内皮细胞增殖、迁移和管状结构形成,并上调VEGFA、PDGFB等血管生成相关基因的表达。
(2)通过将PAP与温敏水凝胶PNPHO共价结合,构建了PAP-co-PNPHO长效缓释系统。该水凝胶具备优秀的机械强度和自愈合能力,可实现40天以上的持续释放。
(3)在小鼠后肢缺血模型中,PAP-co-PNPHO显著恢复血流灌注。术后第7天血流灌注比即显著优于对照组,术后21天肢体保留率达80%。
(4)PAP-co-PNPHO通过上调PDGF-B/PDGFR-β信号通路,促进周细胞募集和血管稳定,实现功能性血管新生。
核心数据展示:
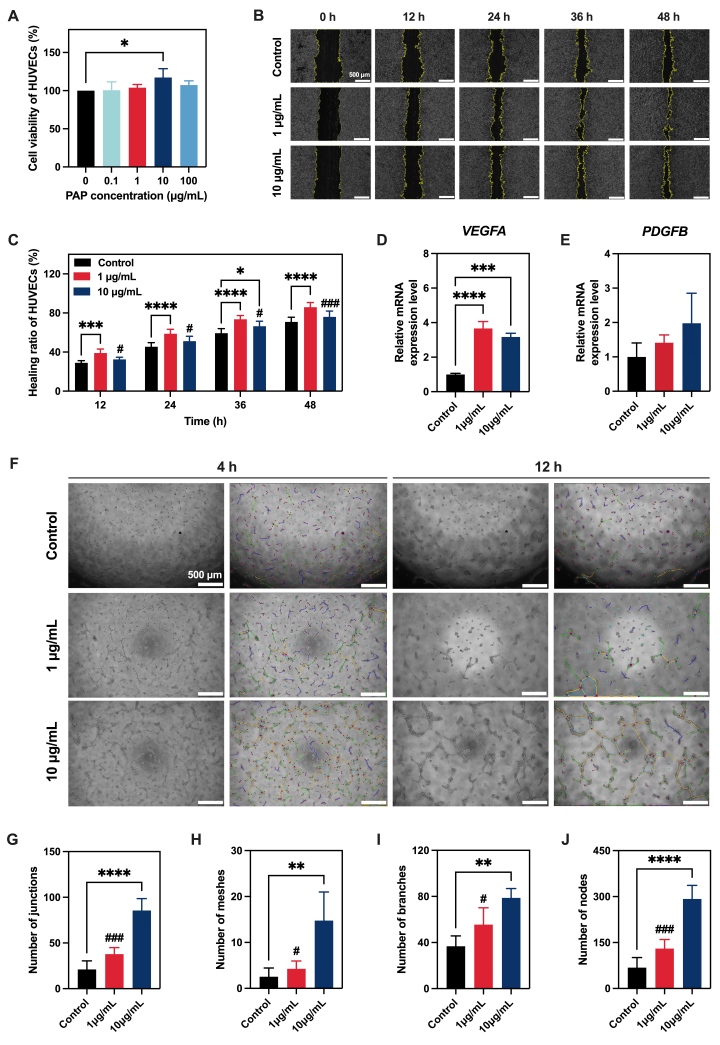
图二、PAP的体外促血管生成活性验证。(A)CCK-8法检测细胞增殖;(B-C)划痕实验检测细胞迁移;(D-E)qRT-PCR检测VEGFA和PDGFB基因表达;(F-J)管状结构形成实验及定量分析。
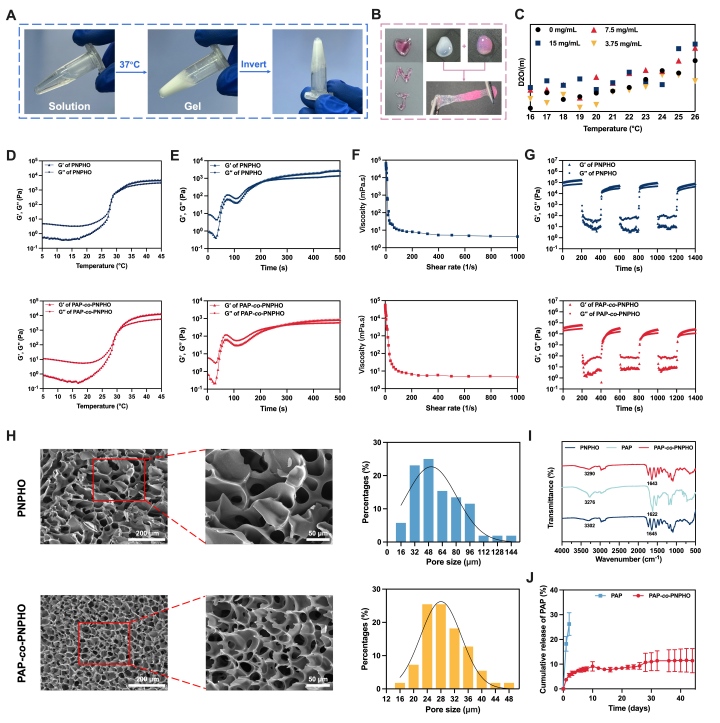
图三、PAP-co-PNPHO水凝胶的性能表征。(A-B)PNPHO水凝胶温敏性和可注射性;(C)PAP与PNPHO最佳耦合浓度的确定;(D-G)流变学分析;(H)SEM微观结构;(I)红外光谱;(J)体外释放曲线。
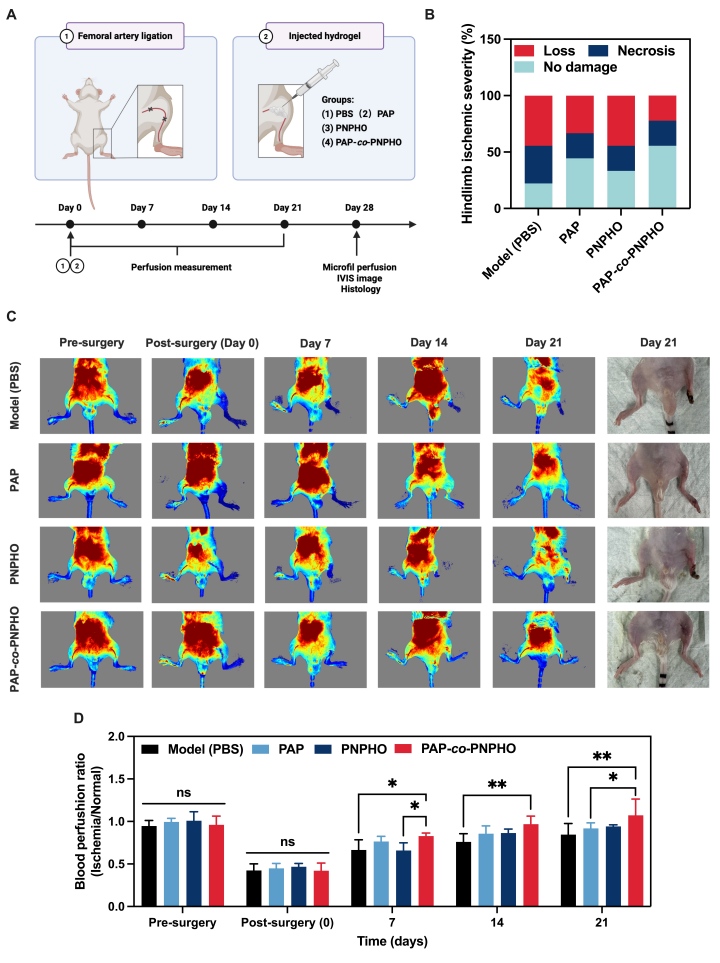
图四、PAP-co-PNPHO在小鼠后肢缺血模型中的疗效。(A)实验设计示意图;(B)术后21天宏观观察;(C-D)激光散斑成像及定量分析。
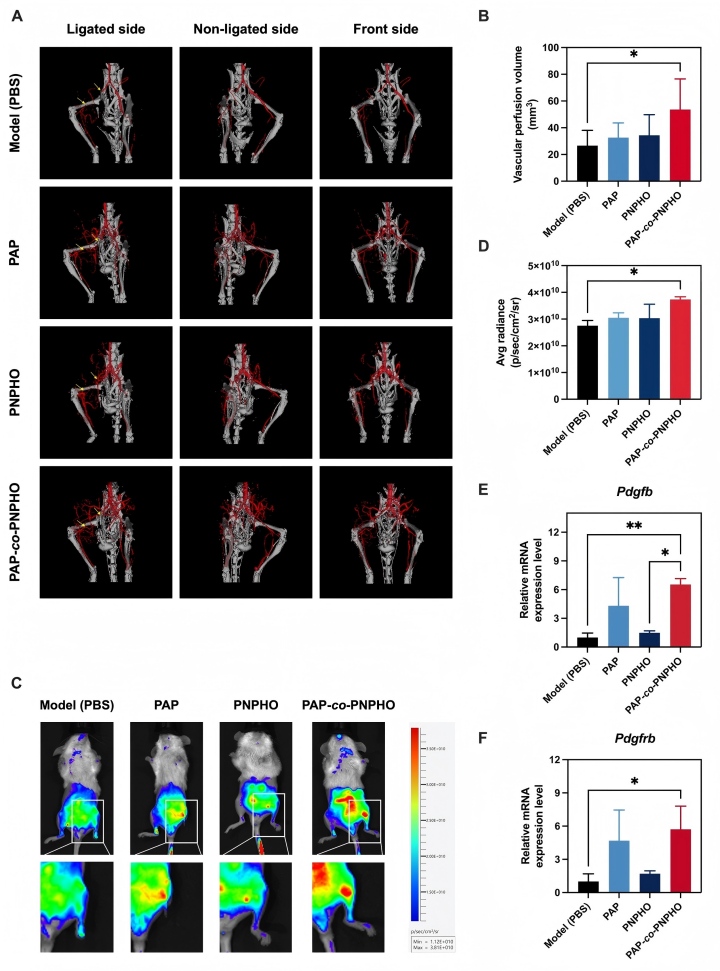
图五、PAP-co-PNPHO促进后肢血管新生与成熟。(A-B)Micro-CT血管重建;(C-D)活体荧光成像;(E-F)PDGF-B/PDGFR-β基因表达。
总结与展望
该研究成功地将传统中药的智慧与现代生物材料技术相结合,构建了一种集“靶向递送、长效释放、生物活性”于一体的新型水凝胶系统PAP-co-PNPHO。它不仅验证了鹿茸多肽作为促血管生成新分子的潜力,更提供了一种具备临床转化潜力的治疗策略,有望为缺血性疾病的治疗提供一种兼具安全性、有效性和便利性的创新方案。
参考文献:
Zhao W, Xue N, Ge Z, Wu Y, Fathi A, Maleknia S, Oveissi F, Liu P, Duan J, Wang Y. Targeted and sustained release of pilose antler peptide from a thermosensitive injectable hydrogel for ischemic tissue repair. Chem Eng J. 2026;534:175160.